¿COMO MEJORAR TU SALUD BUCAL?

¿Cómo mejorar tu salud bucal?
¿Cómo podría cambiarse la acidez del mentol sin alterar el efecto del enjuague bucal?
Para ello se debe analizar los siguientes problemas:
Ø En el enjuague bucal en la mayoría se presenta el mentol el cual causa irritación y frescura al combinar el mentol con el saborizante a fresa ¿podría mejorar su sabor y su calidad?
ü ¿por qué el ácido bórico que contiene el enjuague bucal no quema?
ü ¿Por qué es indispensable el alcohol en la elaboración del enjuague bucal?
ü ¿Qué consecuencias traería la incorrecta agregación de los ingredientes?
ü ¿Se podría utilizar otro saborizante?
ü ¿Qué compuestos tiene el enjuague bucal?
ü ¿Qué es lo innovador en el enjuague bucal respecto a los demás?
ü ¿Cuáles son los pasos para la elaboración del enjuague bucal?
ü ¿Qué consecuencias traería si se llega ingerir al menos una gota del enjuague bucal?
ü Aproximadamente ¿Cuál es el porcentaje de bacterias que elimina?
ü ¿Cómo el saborizante elimina la sustancia fuerte como el alcohol?
ü ¿Qué personas están aptas para utilizarlo?
ü ¿Qué otros usos podría utilizar el ácido bórico?
ü ¿Qué tipo de ácido tiene el enjuague bucal?
ü ¿Qué tipo de alcohol tiene el enjuague bucal?
ü ¿En dónde se puede encontrar el alcohol?
Objetivo General
Demostrar el efecto que tiene el mentol en el enjuague bucal al ser mezclado con el saborizante, dando así respuesta a los planteamientos anteriormente elaborados.
Objetivos Específicos
· Dar a conocer la reacción que tiene el alcohol junto con el ácido bórico.
· Evidenciar que la química está presente en el día a día
· Demostrar que en casa se puede hacer un enjuague bucal
· Optar por el beneficio de las personas que no pueden utilizar un enjuague bucal común.
Justificación
En estos tiempos, el enjuague bucal se ha convertido en uno de los medios o factores que mejor combate enfermedades de la boca, y que ayuda combatir el mal aliento, lo cual demuestra la importancia de su uso. Sin embargo hay que considerar que lamentablemente no todas las personas utilizan este método dentro de su higiene bucal bien sea por desconocimiento del mismo o por no tener el dinero para comprarlo pero esto cambiara cuando demostremos con este proyecto que fácilmente en casa se podrá realizar un enjuague bucal con productos que están a la mano. Buscando siempre el beneficio y la comodidad de las personas al poder utilizar este enjuague.
Así mismo cabe resaltar que con la implementación del enjuague bucal se brindan innumerables beneficios, como eliminar restos de alimentos después del cepillado, suprimir temporalmente el mal aliento, reducir las bacterias y refrescar la boca dejando un sabor agradable.
Marco teórico
Fundamentos teóricos
Alcohol
En química se denomina alcohol a aquellos compuestos químicos orgánicos que contienen un grupo hidróxido (-OH) es decir, un grupo funcional formado por un átomo de oxígeno y otro de hidrogeno característicos de los alcoholes.
Los alcoholes suelen ser líquidos incoloros de olor característico, soluble en el agua en proporciones variables y menos densas que ella. (Daniel Aníbal Galatro , 2010)
Tipos
Los alcoholes pueden ser primarios es decir si el átomo de hidrogeno el cual es sustituido por el grupo hidróxido (-OH) está ubicado en un carbón que a su vez esta enlazado a un solo carbón.
Los alcoholes secundarios son aquellos que el átomo de hidrogeno el cual es sustituido por el grupo hidróxido (-OH) está ubicado en un carbón que a su vez esta enlazado a dos carbones.
Los alcoholes terciarios son aquellos que el átomo de hidrogeno el cual es sustituido por el grupo hidróxido (-OH) está ubicado en un carbón que a su vez esta enlazado a tres carbones.
(Anshul, 2010)
Propiedades químicas de los alcoholes
Deshidratación de alcoholes
La deshidratación de alcoholes es un proceso químico que consiste en la transformación de un alcohol para poder ser un alqueno por procesos de eliminación. Para realizar este procedimiento se utiliza un ácido mineral para extraer el grupo hidroxilo (OH), por esto, la deshidratación de alcoholes es útil, puesto que fácilmente convierte a un alcohol en un alqueno.
Oxidación
La oxidación es la reacción de los alcoholes para producir ácidos carboxílicos, cetonas o aldehídos dependiendo del tipo del alcohol y del catalizador.
Deshidrogenación
Los alcoholes primarios y secundarios cuando se calientan en contacto con ciertos catalizadores, pierden átomos de hidrogeno para formar aldehídos o cetonas. Si esta des hidrogenación se realiza en presencia de aire (O), el hidrogeno sobrante se combina con el oxígeno para dar agua.
Halogenacion
El alcohol reacciona con un halógeno para formar haluros de alquilo más agua.
Deshidratación
Es una propiedad de los alcoholes mediante la cual podemos obtener esteres o alquenos. (Anshul, 2010)
Fuentes
Muchos alcoholes pueden ser creados por fermentación de frutas o granos de levadura, pero solamente el etanol es producido comercialmente de esta manera, principalmente como combustible y como bebida. Otros alcoholes son generalmente producidos como derivados sintéticos del gas natural o del petróleo. (sabelotodo)
Usos
Los alcoholes tienen una gran gama de usos en la industria y en la ciencia como disolventes y combustibles. (anshul, 2010)
Alcohol del Botiquín
El alcohol del botiquín puede tener varias composiciones. Puede ser totalmente alcohol etílico al 96°, el cual es un alcohol que se presenta en condiciones normales de presión y temperatura como un líquido incoloro e inflamable con un punto de ebullición de 78,4°C, cuya fórmula química es CH3-CH2-OH, con algún aditivo como el cloruro de benzalconio, el cual es un desinfectante o alguna sustancia para darle un sabor desagradable. ( Alarkn y PiNzon , 2010)
Nomenclatura
Se nombran con la terminación “-ol”, e indicando con un numero la posición del alcohol.
· Según la posición del carbono que sustenta el grupo –OH, lo alcoholes se denominan primarios, secundarios o terciarios.
· Si en la molécula hay más de un grupo –OH, se utiliza la terminación “-diol”, “-triol”. Indicando con números las posiciones donde se encuentra los alcoholes.
· Cuando el alcohol no es la función principal, se nombra “hidroxi-“.
Indicando el número correspondiente.
(alonsoformula@gmail.com, 2015)
Mentol
El mentol es un alcohol secundario saturado, que se encuentra en los aceites de algunas especies de menta, principalmente en Mentha Arvensis; el cual es una especie de planta fanerógama cuyo grupo de plantas son ancestrales, perteneciente a la familia Lamiaceae, el cual es un grupo de plantas con flores del orden Lamiales, cuyo origen es de familia nativa de las regiones templadas de Europa y Asia central y Occidental.
El mentol es un sólido cristalino que funde alrededor de los 40°C y que se emplea en medicina y en algunos cigarrillos ya que posee un efecto refrescante sobre las mucosas; el cual es la capa formada por el epitelio siendo este el tejido formado por una o varias capas de células unidas entre sí, que puestas recubren todas las superficies libres del organismo, que reviste las paredes internas de los órganos que están en contacto con el exterior del cuerpo.
El mentol es insoluble en agua y soluble en alcohol y éter. Se puede obtener tanto sintéticamente como de la naturaleza (menta). (Iqb, 2010)
Se utiliza como ingrediente en los siguientes tipos de productos
· En las cremas dentales
· En los chicles
· En medicamentos para el herpes labial(fuegos)
· En los ungüentos para tratar dolores y congestiones nasales
· En las cremas y lociones para aliviar la picazón
· En los enjuagues bucales
( Sarah Terry , 2013)
Sobredosis del mentol
Se pueden presentar los siguientes síntomas
· Vejiga y riñones
- Sangre en la orina
· Pulmonares
- Respiración superficial
- Puede también ser rápida
· Gastrointestinales
- Dolor abdominal
- Diarrea
- Nauseas
- Vómitos
· Cardiovasculares
- Latidos cardiacos rápidos
· Sistema nervioso
- Perdida del conocimiento
· Mareo
· Convulsiones (medicina herbaria)
A
ANTECEDENTES DEL ENJUAGUE BUCAL
pa La necesidad de mantener una boca limpia se relaciona directamente con la salud, por lo que es preciso cuidar la higiene en este sentido.
Eso lo supo bien Anton van Leeuwenhoek, quien experimentando descubrió que en los dientes llegaban a habitar organismos vivos, los cuales posteriormente serían llamados placa bacteriana, y que era necesario exterminar para garantizar tener una boca saludable.
En un primer intento, Anton probó el erradicarlos con una mezcla de vinagre y brandy, y aunque en laboratorio los organismos eran inmovilizados, al probar consigo mismo descubrió que continuaban en los dientes.
Esos fueron los primeros registros de lo más similar al enjuague bucal, el cual surgiría en base a los esfuerzos de 1865 del doctor Joseph Lister, quien en sus intentos por erradicar los focos de infección durante las operaciones quirúrgicas, dio con los antisépticos.
Para 1879, otro médico llamado Joseph pero de apellido Lawrence, retomó la idea de Lister y mejoró su antiséptico, bautizándolo como Listerine, en honor a su creador.
En 1895 se decidió ampliar el uso de ese producto al ámbito odontológico, formalizándose la creación del primer enjuague bucal, el cual para 1900 ya se vendía libremente en droguerías y farmacias.
Los enjuagues bucales son habitualmente soluciones hidroalcohólicas, esto es, mezclas de alcohol y agua. La concentración de etanol utilizada oscila entre el 4 y el 17 por ciento.
Uno de los aromas más utilizados en los enjuagues bucales es el mentol por la sensación de frescor que deja. Sin embargo, no se recomienda la utilización de mentol en concentraciones superiores al 2 %, ni su uso en productos cosméticos en productos destinados a niños menores de tres años.
Existe la creencia de que a mayor cantidad de enjuague y menor de agua, mayor eficacia como enjuague. Sin embargo, la composición del enjuague sin diluir es demasiado agresiva para la mucosa bucal y esto puede hacer que se produzcan incluso quemaduras químicas en lengua o mucosas.
¿Con o sin alcohol? Algunos dentistas, recomiendan los enjuagues bucales sin alcohol, ya que los que sí lo contienen pueden provocar excesiva sequedad en la boca, y dicha sequedad puede provocar un incremento de actividad bacteriana. Además, creen que el alcohol en sí mismo no tiene capacidad antiséptica en la boca.
El alcohol se emplea como disolvente de los principios del enjuague bucal. Por otro lado, tiene un efecto dañino el cual destruye los tejidos en la cavidad oral, y además, en concentraciones elevadas, puede provocar dolor oral. Su uso está especialmente contraindicado en niños.
Un enjuague bucal se considera más correcto cuanto más se acerque al PH de la cavidad oral, que se encuentra en torno a 7 (ya que si está por debajo del 5,5 el esmalte de los dientes se desmineraliza y su estructura comienza a estropearse). Como todos los enjuagues son ácidos, deben usarse preferentemente justo tras el cepillado, ya que en ese momento el pH de la boca es ligeramente alcalino (el cual es el balance de una sustancia, PH) y estos elixires (es un líquido de sabor dulce para curar enfermedades) ayudan a equilibrarlo. (editora de la laguna, 2014)
Bibliografía
Alarkn y PiNzon . (2 de septiembre de 2010). blogspot. Obtenido de blogspot: http://alarknypinzon.blogspot.com.co/2010/09/alcohol-de-botiquin.html
Sarah Terry . (2013). livestrong. Obtenido de livestrong: http://www.livestrong.com/es/del-mentol-sobre_16085/
alonsoformula. (s.f.). Obtenido de http://www.alonsoformula.com/organica/alcohois.htm
alonsoformula@gmail.com. (26 de mayo de 2015). alonsoformula.com. Obtenido de alonsoformula.com: http://www.alonsoformula.com/organica/alcohois.htm
anshul. (2010). blogger. Obtenido de blogger: http://alcoholesquimica.blogspot.com.co/2010/10/usos-del-alcohol.html
Anshul. (2010). blogger blogger template. Obtenido de blogger blogger template: http://alcoholesquimica.blogspot.com.co/
Bioquimico Patricio Arroyo. (23 de mayo de 2011). quimica y algo mas. Obtenido de quimica y algo mas: http://www.quimicayalgomas.com/quimica-organica/acidos-organicos-parte-1/
Daniel Aníbal Galatro . (2010). conceptos de quimica. Obtenido de conceptos de quimica: http://conceptosdequimica.blogspot.com.co/2010/04/alcoholes-propiedades-generales-y.html
ecured@idict.cu. (25 de julio de 2016). Ecured. Obtenido de Ecured: http://www.ecured.cu/%C3%81cido_b%C3%B3rico
editora de la laguna. (11 de septiembre de 2014). el siglo de torreon. Obtenido de el siglo de torreon: https://www.elsiglodetorreon.com.mx/noticia/1036314.el-enjuague-bucal-datos-breves-sobre-sus-origenes-e-historia.html
Gonzales, M. (s.f.). Quimica II. publicaciones cultural Ltda.
Iqb. (17 de marzo de 2010). Iqb/monografia. Obtenido de Iqb/monografia: http://www.iqb.es/monografia/fichas/ficha104.htm
medicina herbaria. (s.f.). salud y bienestar. Obtenido de salud y bienestar: http://lasaludi.info/efectos-secundarios-de-mentol.html
plantilla Ethereal/ AHM. (5 de agosto de 2007). blogger/seguridad profesiones y productos quimicos. Obtenido de blogger/seguridad profesiones y productos quimicos: http://profesionseg.blogspot.com.co/2007/08/usos-de-los-acidos-organicos.html
sabelotodo. (s.f.). sabelotodo.org. Obtenido de sabelotodo.org: http://www.sabelotodo.org/quimica/alcoholes.html
HIPOTESIS
Si el enjuague bucal elaborado en este proyecto es de calidad entonces al momento de utilizarlo en el hogar será efectivo porque se utilizó un método para identificar el PH.
Si el enjuague bucal es ingerido producirá dolores estomacales porque no es apto para el organismo.
METODOLOGIA
El primer intento disolvimos el mentol con una cantidad de 0.02g equivalente a 2 gotas de un gotero de vidrio, el saborizante de fresa con 0.6g y el alcohol con 20g en un vaso de 7 onzas.
Continuamos disolviendo el ácido bórico con una cantidad de 2.0g en agua con una cantidad de 100 mililitros.
Por ultimo mesclamos las dos soluciones obtenidas anteriormente y le probamos el PH el cual nos dio neutro es decir PH 7.
Pero este primer intento vimos que tanto el saborizante como el mentol no se sentía.
El segundo intento disolvimos el mentol con una cantidad de 15g, el saborizante de fresa con 0.6g y el alcohol con 20g en un vaso de 7 onzas.
Continuamos disolviendo el ácido bórico con una cantidad de 2.0g en agua con una cantidad de 100 mililitros.
Por ultimo mesclamos las dos soluciones obtenidas anteriormente y le probamos el PH el cual nos dio neutro es decir PH 7.
Pero este segundo intento se sintió mucho el mentol dando un toque acido al enjuague bucal y como este no es el objetivo del proyecto toco medir otra vez las cantidades.
En el tercer intento disolvimos el mentol con una cantidad de 78g, el saborizante de fresa con 150g y el alcohol con 30g en un vaso de 7 onzas.
Continuamos disolviendo el ácido bórico con una cantidad de 10g en agua con una cantidad de 100 mililitros.
Por ultimo mesclamos las dos soluciones obtenidas anteriormente y le probamos el PH el cual nos dio neutro es decir PH 7
Este tercer y último intento quedo equilibrado tanto el mentol y el saborizante, pero quedando este último con un toque más.
|
|
Mentol (g) |
Agua (ml) |
Saborizante(g) |
Alcohol (g) |
Ácido Bórico |
|
1° intento |
0.02 |
100 |
0.6 |
20 |
0.02 |
|
2° intento |
15 |
100 |
0.6 |
20 |
2.0 |
|
3° intento |
78 |
100 |
150 |
30 |
10 |
Los materiales que se utilizara para este enjuague bucal son:
· Saborizante sabor a fresa
· Alcohol
· Mentol
· Ácido bórico
· Agua
· Dos vasos de plástico de 7 onzas
· Un gotero de vidrio
· Una gramera
· Un tenedor de plástico
· Un medidor de PH
Utilizamos una gramera para medir las cantidades de los ingredientes además de un gotero de vidrio comprobándolo por el método organoléptico es decir por medio de los sentidos en específico el olor y el color dando así el resultado esperado del enjuague bucal.
¿Cómo hacer un acido milagroso para la salud?


Objetivos
General
· Analizar y determinar los compuestos y procesos químicos que permiten que el vinagre de manzana tenga diversos beneficios para la salud de las personas.
Específicos-CORREGIR
· Estudiar los diferentes componentes de los ingredientes del vinagre de manzana para que estos combinados den un resultado beneficioso para la salud de las personas.
· Establecer y relacionar las distintas reacciones de obtención con los compuestos orgánicos del vinagre de manzana.
· Definir las propiedades físicas y químicas que se producen o se evidencian en la elaboración del vinagre de manzana
Justificación
Con el vinagre de manzana se busca determinar y relacionar las propiedades físicas y químicas y las reacciones de obtención involucradas al momento de su elaboración y con estos aspectos establecer como estos compuestos actúan dentro del organismo humano produciendo beneficios para la salud.
MARCO TEORICO
En la alimentación diaria se consumen una infinidad de alimentos y de estos en muchos casos no se conoce el origen ni el tratamiento, con el pasar del tiempo la tecnología se ha ido expandiendo tanto que incluso en la comida ya vemos grandes cambios en comparación a años pasados, en muchos de estos casos los alimentos que consumimos son perjudiciales para la salud sin saberlo, pero otros que aún conservan los métodos manuales o naturales de cultivo y producción generalmente conservan más sus beneficios para la salud de las personas, entre ellos están las frutas que son un tipo de alimento que aún conservan estos procedimientos naturales. En el caso de nuestro proyecto fueron usadas las manzanas como producto orgánico para la elaboración del vinagre.
En la producción del vinagre de manzana se hace presente el proceso de fermentación el cual consiste en la transformación de las moléculas en un tipo de moléculas más simples, en este caso las moléculas de la manzana se simplifican en el proceso y conjuntamente de este se presenta un proceso anaeróbico el cual se refiere a que no tiene presencia de oxígeno. En el caso del vinagre de manzana se ve inicialmente una fermentación alcohólica y posteriormente el resultado y el sumo de la manzana del vinagre, de esto se realiza una fermentación acética que nos deja como producto el ácido acético, pero además de estos se forman otros ácidos que son grasos como son el ácido fenico y el ácido valeriánico estos combinados con residuos del alcohol forman éteres y todos estos productos contribuyen a dar el aroma del vinagre.
Los ácidos inorganicos son, compuestos donde hay mayor concentracion de átomos de hidrogeno. Los ácidos inorgánicos que se pueden obtener son:
1. Elementos químicos bien sea de la combinación de hidrógenos con un elemento no metálico o un halógeno (F, Cl, Br, I). Estos son nombrados como hidrácidos, formula general: HnX (donde X es el elemento no metálico y n es la valencia de dicho elemento).
2. De la combinación de agua con un elemento no metálico, estos son nombrados como oxácidos, formula general: no metálico +H2O HaXbOc
(Donde X es un no metal o un metal de transición)
La otra clase de ácidos que
podemos encontrar son los
ácidos orgánicos, los cuales
se obtienen de la combinación
de oxígenos con otros
elementos químicos, entre
ellos se encuentran:
- Monocarboxílicos : Se forman cuando dos átomos de hidrogeno son sustituidos por un átomo de oxigeno y por un hidroxilo (-OH), en un carbono primario de un hidrocarburo. Formación general : Ácido + Hidrocarburo, con terminación ´´-oico``
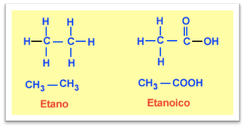
(Deza, 2008)
2. Dicarboxílicos : Se caracteriza por tener dos grupos carboxílicos (- COOH).
La fórmula general de un ácido dicarboxílico es : HOOC-R-COOH
Formulación general : Acido + Hidrocarburo con terminación ‘’-dioico’’

(Químicas)
3. Tricarboxílicos : Se caracteriza por tener grupos carboxílicos (-COOH).
1
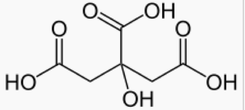
(Wikipedia, 2009)
Los resultados que se pueden obtener de estos compuestos por lo general tienen como característica la capacidad de diluir otros compuestos por su gran grado de acidez, generalmente las personas al escuchar ácidos siempre lo relacionan con esta característica que se podría llamar destructiva, pero en el caso del vinagre de manzana el ácido que se encuentra en él tiene grandes beneficios para la salud de las personas.
Puesto a ser un compuesto orgánico este está conformado por el ácido acético cuya fórmula es CH3-COOH o de forma empírica CH2O, antioxidantes y aminoácidos y también pequeñas cantidades de vitaminas, minerales y calorías que le dan esas propiedades beneficiosas para el consumo humano como son la capacidad de reducir la glucosa en la sangre lo cual provoca una mejor asimilación a la insulina dependiendo el tipo de grado de diabetes que se tenga, este producto también ayuda a proteger contra la oxidación de partículas de colesterol, etc.
ANTECEDENTES
En 1847, el químico alemán Hermann Kolbe sintetizó el ácido acético por primera
vez a partir de elementos orgánicos, dejandole una secuencia de reacciones :
- Cloración de carbono para obtener tetracloruro de carbono.
- Pirolisis produciendo tetrafluoretileno.
- Cloración en disolución acuosa para dar ácido tricloroacético.
- Reducción electrolítica a ácido acético.
Vinagre de sidra :
Según MORALES, (1971), este tipo de vinagre es proveniente de la fermentación de bebida preparada con jugo de manzana.
Para la preparación se debe tener en cuenta que :
Las manzanas utilizadas deben encontrarse en estado óptico de madurez conteniendo aproximadamente de 8 a 10 % de azúcar. Este tipo de vinagre es el más popular en los Estados Unidos de Norteamérica, debido a que es usado por los pacientes que sufren de artritis.
´´Las características del vinagre de manzana en óptimas condiciones deben ser:
-Densidad 1,012 a 1,014
-Acidez fija expresado en ácido málico : 0,11 %
-Extracto seco : 1,4 % a 1,7 %
-Acidez total expresado en ácido acético : 3 a 4 %
-Relación media entre la acidez y el extracto : 1,94
-Bitartrato de potasío no contiene
-Cenízas : 0,25 % ``
(YAMADA, 2009)
Producción industrial de Vinagre
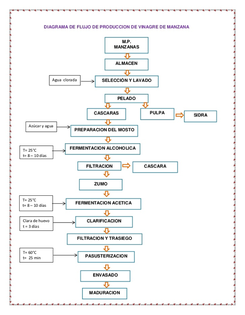
(hurtado, 2012)
Como se aprecia en el diagrama de flujo anterior a nivel industrial se lleva un proceso un poco más elaborado a comparación del método el cual se está usando en este proyecto.
En este tipo de producción se muestra como las condiciones de aire y temperatura son estandarizados y perfectamente controlados para que el producto no tenga ningún riesgo de perdida.
Ejemplo :

Producción casera del vinagre
En el caso del vinagre de manzana casero que es el que se está implementando en este proyecto, tipo de producción los estándares como son:
· La temperatura de almacenamiento se mantienen sujetos al ambiente y al clima del territorio es decir al estar almacenado a temperatura ambiente dependiendo del clima del territorio va a variar.
· El ser casera la elaboración el periodo de tiempo se extiende a dos meses para que alcance un punto de acides adecuado.
· La cantidad producida siempre será reducida.
El proceso de producción la secuencia casi siempre se mantiene, pero se han encontrado diversos cambios o modificaciones en el proceso que son opcionales.
Ejemplos :
· Las personas tienen la opción de implementar a la preparación un alimento rico en azúcar puesto a que este ayuda a la aceleración de la fermentación puede ser la panela o la miel.
· En muchos casos al momento se cortas las manzanas se introducen directamente en el agua para empezar la preparación, pero las personas tienen la opción de esperar unos minutos después de cortarlas para que estas se oxiden un poco con el contacto del aire
· Al momento producir vinagre se puede tener la opción de cambiar la manzana por otras frutas como la piña o uvas etc.
Gel para masajes

¿COMO RELAJAR NUESTROS MÚSCULOS?
- DEFINICIÓN AL PROBLEMA:
¿Cómo sabemos si el alcohol no genera una reacción a nuestro gel?
OBJETIVOS:
· Realizar nuestro gel obteniendo una consistencia ideal para nuestro producto
· Obtener el PH adecuado en nuestro gel para que sea confiable a nuestros clientes
· Mantener el sistema nervioso sano
· Eliminar la acumulación de grasa localizada y a la vez estilizar el contorno de la figura
· Calma dolores musculares y contribuye a la relajación
· Buena calidad , a bajo precio obteniendo cualquier tipo de sugerencia del consumidor
· Explicar los diferentes parámetros que incluyen este producto
JUSTIFICACIÓN:
Vamos a realizar un gel para masajes que destaca la importancia de relajar a las personas que por diferentes causas han llegado al punto del estrés, se escogió este gel para masajes color verde con aroma a fresa el cual consiste en relajar, mejorar pieles cansadas, apagadas y con falta de hidratación con el fin de desarrollar una efectividad a la comunidad ya que en nuestro entorno de vida nuestros músculos están expuestos a diferentes movimientos no agradables y esto va generar un efecto relajante gracias al calor que se obtendrá por los masajes .
MARCO TEÓRICO -CORREGIR
Alcoholes: son un compuesto orgánico que en el cual tienen un hidroxilo (-OH) este se encuentra unido a una cadena hidrocarbonada que a través de un enlace covalente a un átomo de carbono con hibridación sp3.
(grupoalcholes, 2011)
¿como hacer luz neón?

Planteación del Problema:
Los derivados de los fenoles sufren reacciones de oxidación en presencia de catalizadores como el peróxido de hidrogeno, cobre y hierro en las cuales la energía sobrante de esta reacción se convierte en un proceso quimioluminiscente.
Objetivo General:
-Analizar y comprender el proceso químico de compuestos orgánicos para producir reacciones que puedan generar luminiscencia
Objetivos Específicos:
- Definir y comparar los diferentes tipos de Luminicencia que se pueden generar
-Identificar y establecer diferencias en la utilización de otras sustancias además del Luminol como Rodamina 6G y Rubreno
-Desarrollar diferentes procesos para obtener quimioluminiscencia
-Determinar los resultados de cada proceso de producción de quimioluminiscencia que permita describir sus propiedades físicas y químicas
Justificación:
Este proyecto se ha diseñado con la finalidad de dar a conocer la quimioluminiscencia y como componentes como los derivados del fenol crean una reacción química lumínica.
El proyecto puntualiza los temas referentes a las reacciones que comprenden tanto a los catalizadores como los compuestos cuya reacción van a dar origen a la producción de quimioluminiscencia, además va a tratar de describir los procesos de la bioluminiscencia profundizando en ellos, para así poder identificar la forma de obtener luz neón de manera química.
Marco Teórico
“¿Cómo hacer galletas para mascotas?

Ayudamos al medio ambiente convirtiendo los residuos en comida para mascotas, evitando así la contaminación.
Objetivo general:
Ayudar al medio ambiente, dándole uso a los residuos de los restaurantes que van a parar a la basura, alimentando así a las mascotas de una manera segura e higiénica.
Objetivos específicos:
-Recolectar los residuos alimenticios de los restaurantes, impidiendo la degradación de estos.
-Dar un nuevo uso a los residuos recolectados, evitando la contaminación del medio ambiente.
-Implementar y mejorar los hábitos y costumbres en la recolección y la eliminación los desechos orgánicos.
Justificación:
La comida en descomposición genera gases tóxicos como lo es el gas metano que se produce a partir de la descomposición de los compuestos orgánicos el cuales afecta tanto al ser humano como al medio ambiente. Se reduce la reproducción de algunos insectos y plagas que pueden llegar a causar diversas enfermedades tales como la peste bubónica la cual se transmite por medio de una mordida que es generada por el ratón. Se genera conciencia sobre el reciclaje de comida orgánica. Se evita la contaminación del agua ya que hay comida que contiene mercurio, el cual aumenta a medida que se desecha comida. Hace un aporte a la comunidad Villetana para mejorar la calidad de vida de las mascotas, con el fin de reducir la contaminación orgánica convirtiéndola en comida para mascotas.
Hipótesis
Generar un nuevo uso a los desechos alimenticios recolectados en los restaurantes y casas convirtiéndolos en comida para perros evitando así que estos terminen en basuras generando gases tóxicos que contaminan al medio ambiente y producen enfermedades a los seres humanos.
Se elaborará un secador solar para llevar a cabo así el secado de la comida ya convertida en croquetas, buscando así la conservación de estas y evitando la perdida de diversas proteínas y vitaminas que puede causar un horno convencional, además también queremos aportar a la no contaminación del medio ambiente ya que este no usa ningún tipo de gas o de energía contaminante.
¿CÓMO PREPARAR UNA MASCARILLA CONTRA EL ACNE?

EN LA ACTUALIDAD LOS JÓVENES Y ADULTOS SUFREN A CONSECUENCIA DE LA APARICIÓN DE IMPERFECCIONES COMO EL ACNÉ Y PUNTOS NEGROS QUE ALTERAN LA ESTÉTICA Y EL AUTOESTIMA DE ESTOS. TAMBIÉN A CAUSA DE LA EXPOSICIÓN SOLAR APARECEN EN LA PIEL AFECTANDO SU APARIENCIA GENERANDO UN COLOR MAS OSCURO EN ALGUNAS ZONAS DEL ROSTRO.
LLUVIA DE IDEAS
- ¿POR QUÉ EL CARBÓN ACTIVO ABRE LOS POROS?
- ¿SI FALTA ALGÚN INGREDIENTE FUNCIONA IGUAL LA MASCARILLA?
- ¿QUÉ FUNCIÓN CUMPLE LA LECHE?
- ¿CUÁL ES LA FUNCIÓN DE LA GELATINA EN ESTA MESCLA?
- ¿QUÉ PASA SI SE CALIENTA MÁS DE LA TEMPERATURA DE LA RECETA?
- ¿POR QUÉ LA PIEL PRODUCE GRASA?
- ¿QUÉ HACE QUE EL CARBÓN SEA ACTIVO?
- ¿SE PUEDE REMPLAZAR LA GELATINA POR OTRO ELEMENTO?
- ¿SE PUEDE USAR OTRO TIPO DE GELATINA?
- ¿SIRVE CON CUALQUIER TIPO DE LECHE?
- ¿QUÉ PASA SI LA MASCARILLA SE RETIRA ANTES DE QUE ESTE SECA?
- ¿SI SE AGREGA MÁS O MENOS DE UN INGREDIENTE QUE PASA?
OBJETIVOS
ESPECIFICO:
GENERAR UN PRODUCTO EFECTIVO EN CONTRA DE LA APARICION DE ACNE EN LOS JOVENES Y ADULTOS, CON PIELES GRASAS Y MIXTAS, A BASE DE PRODUCTOS NATURALES Y DE FACIL ADQUISICION
GENERAL:
- ENSEÑAR A LAS PERSONAS UNA FORMA FACIL PARA LIMPIAR SU CARA
- DAR A CONOCER LA EFECTIVIDAD DEL CARBÓN ACTIVO EN LA PIEL DEL ROSTRO
- DAR A CONOCER LA EFECTIVIDAD DEL CARBÓN ACTIVO EN LA PIEL DEL ROSTRO
- DEMOSTRAR QUE NUESTRA MASCARILLA GENERA UN BENEFICIO A NIVEL CUTANEO E INTERNO DE LA PIEL ELIMINANDO LA APARICION DE IMPERFECCIONES
- DEMOSTRAR COMO CONTRIBUYE LA LACTOSA PARA MEJORAR EL ASPECTO DE LA PIEl
- DEMOSTRAR COMO CONTRIBUYE LA LACTOSA PARA MEJORAR EL ASPECTO DE LA PIEl
-CONOCER TODOS LOS BENEFICIOS QUE CONLLEVA EL USO DE CARBÓN ACTIVO, LACTOSA Y GELATINA EN LA PIEL
- MOSTRAR QUE ESTE PRODUCTO DEBE CONTAR CON UNA TEMPERATURA LA CUAL EN PRIMERA LUGAR UNIFICA LA MESCLA Y EN SEGUNDO LUGAR ESTIMULA LA APSORCION DE LOS BENEFICIOS DE LA MISMA POR LA PIEL
JUSTIFICACIÓN:
ESTE PROYECTO PRODUCE UN COSMÉTICO INNOVADOR DIRIGIÉNDOSE EN ESPECIAL A LOS JÓVENES A QUIENES EL ACNÉ SE CONVIERTE EN UNA DIFICULTAD IMPORTANTE YA QUE EN MUCHAS OCACIONES BAJA EL AUTOESTIMA DE QUIENES LO SUFREN
PENSANDO EN LA CONSERVACIÓN Y CUIDADO DE LA SALUD EN LOS JÓVENES SE HA TRABAJADO CON BASE EN LA UTILIZACIÓN DE PRODUCTOS NATURALES Y APORTAN AL CUIDADO DE LA PIEL SIN CAUSAR EFECTOS NOCIVOS.
LOS ELEMENTOS SELECCIONADOS PARA ESTE PROYECTO GARANTIZAN QUE EL PRODUCTO PUEDA SER ELABORADO CON GRAN FACILIDAD POR LA FÁCIL ADQUISICIÓN EN EL MERCADO DE LOS INGREDIENTES. ESTO GENERA COMO CONSECUENCIA EL GARANTIZAR A LOS JÓVENES UN USO PERMANENTE QUE VA A DAR SUS FRUTOS EN LA CONSECUCIÓN DE UNA PIEL LIMPIA DE IMPUREZAS COMO LO DESEA TODA PERSONA AÚN MÁS EN ESTA EDAD DE JUVENTUD
DURANTE MUCHO TIEMPO LAS PERSONAS HAN SUFRIDO DE IMPUREZAS EN LA PIEL, ESTO AFECTA SU AUTOESTIMA E INCLUSO LLEVA A EL AISLAMIENTO CON EL FIN DE NO MOSTRARSE A NADIE .
LA MASCARILLA NEGRA O PEELOFF BRINDA A LOS QUE LA USAN UNA HERRAMIENTA PARA ELIMINAR DICHAS IMPERFECCIONES DE UNA MANERA MAS FÁCIL Y PRACTICA.
PARA SU ELABORACIÓN NECESITAS MATERIALES MUY FÁCILES DE OBTENER:
COMO LA LECHE QUE CONTIENE LACTOSA, LA LACTOSA ES EL AZÚCAR DE LA LECHE, UNO DE LOS PRIMEROS DESCUBRIMIENTOS DE LA LACTOSA FUE ECHO POR UN FÍSICO LLAMADO FABRIZIO CUYO ORIGEN ES ITALIANO PUBLICADO EN 1633, MUCHOS CIENTÍFICOS Y FARMACÉUTICOS HAN PUBLICADO DISTINTAS INFORMACIONES ACERCA DE LOS BENEFICIOS Y CONTRAS DEL AZÚCAR DE LA LECHE, TAMBIÉN SE HA DICHO QUE UNO DE LOS PRODUCTOS DE LA HIDROLIZACION EN LA LACTOSA ES LA GLUCOSA.
HTTPS//ES.M.WIKIPEDIA.ORGL
TAMBIÉN TENEMOS LA GELATINA SIN SABOR ES UN COLOR OBTENIDO A PARTIR DEL HALOGENO DE ORIGEN ANIMAL TRATADO CON AGUA.
ES UNA PROTEÍNA EN ESTADO PURO, SU FUNCIÓN ES CUAJAR O COMPACTAR A UNA TEMPERATURA AMBIENTE, TAMBIÉN POSEE LA HABILIDAD DE COMPORTARE Y VOLVERSE ACUOSA, LO CUAL ES LLAMADO TERMOREVERSIBLE
PODEMOS OBSERVAR QUE UNO DE LOS INGREDIENTES PRINCIPALES ES EL CARBÓN ACTIVO, QUE POSEE MICROPOROS Y POSEE MUCHOS USOS BIEN SEAN MÉDICOS PARA LA DESINTOXICACION EN PACIENTES, EN EL TRATAMIENTO DE AGUAS PARA PURIFICARLAS EN FILTROS DE AIRE, EN EL ÁREA DE BELLEZA ES UNO DE LOS ENCARGADOS DE REMOVER AQUELLAS TOXINAS Y BACTERIAS QUE POSEE LA PIEL COMO LA PROPIBACTERIUM ACNESPIO, ES IDEAL PARA ECHARSE EN LA PIEL GRASOSA Y MIXTA CON GRAN PROBLEMÁTICA DE ACNÉ. SU FUNCION ES ABSORBER ACEITE MAS QUE NINGUN OTRO INGREDIENTE.UTILIZADO EN LIMPIEZA DE PIEL.
ANTECEDENTES
MUCHAS EMPRESAS QUE SE DEDICAN A EL FABRICA MIENTO PARCIAL HAN CREADO SU PROPIA VERSIÓN COMO:
VOGUE: QUIEN A CREADO NO SOLO MASCARILLAS SINO TOLLAS LIMPIADORAS, ESPONJAS DE CARBÓN Y MUCHOS MAS PRODUCTOS USANDO COMO PRINCIPAL EL CARBÓN ACTIVO.
YOUTUBE: MUCHOS GURUS DE BELLEZA HAN ECHO PARTE DEL BOOM DEL CARBÓN ACTIVO Y LA MASCARILLA NEGRA POR ENDE PRACTICA DISTINTAS TÉCNICAS EN SU ELABORACIÓN.
SE ORIGINO EN KOREA POR UNA MARCA DE BELLEZA LLAMADA DAISON JAPAN, DISEÑA BAJO UN PRECIO ECONÓMICO Y ACCESIBLE.

¿COMO TAPAR GOTERAS DE UNA MANERA FÁCIL Y DIVERTIDA?
DEFINIR EL PROBLEMA
¿Qué beneficios obtiene el medio ambiente con este proyecto?
LISTA DE PREGUNTAS LLUVIA DE PREGUNTAS INCOMPLETA
I. ¿Cuál es la fórmula química y física de la gasolina y el icopor?
II. ¿Cuáles son las características de la gasolina y el icopor?
III. ¿Porque funciona con estos dos compuestos y no con otros?
IV. ¿Cuánto tiempo tarda el icopor en diluirse en la gasolina?
I. ¿Qué es la gasolina?
II. ¿Cuál es el nombre químico de la gasolina?
III. ¿Cuál es la fórmula química de la gasolina?
IV. ¿Cuáles son las características de la gasolina?
V. ¿Cuáles son las propiedades físicas de la gasolina?
VI. ¿Cuáles son las propiedades químicas de la gasolina?
VII. ¿Por cuales compuestos se puede reemplazar la gasolina?
VIII. ¿Cuál es la aplicación de la gasolina?
IX. ¿Qué es el icopor?
X. ¿Cuál es el nombre químico del icopor?
XI. ¿Cuál es la fórmula química del icopor?
XII. ¿Cuáles son las características del icopor?
XIII. ¿Cuáles son las propiedades físicas del icopor?
XIV. ¿Cuáles son las propiedades químicas del icopor?
XV. ¿Por cuales compuestos se puede reemplazar el icopor?
XVI. ¿Por qué este experimento funciona con estos compuestos y no con otros?
XVII. ¿Cuánto tiempo tarda el icopor en diluirse en la gasolina?
OBJETIVOS
OBJETIVO GENERAL
I. Mitigar el impacto ambiental de los residuos plásticos provenientes de empaques de los electrodomésticos
OBJETIVOS ESPECÍFICOS
I. Mitigar una problemática como lo son las goteras en el tejado y así dar solución efectiva y resistente ante cualquier adversidad climática.
II. Dar a conocer la reacción que produce la gasolina con el icopor.
III. Ejecutar con materiales sencillos y de fácil alcance una herramienta divertida y efectiva para los hogares.
IV. Demostrar como este producto contribuye al mejoramiento del medio ambiente.
JUSTIFICACIÓN
I. Para poder explicar lo que sucede en nuestro experimento empezaremos hablando sobre la capacidad que tiene una sustancia de disolver otra para así poder adquirir diferentes conocimientos sobre ello ya que nos permitirá ver la eficiencia de la gasolina al efectuar una reducción o disolución de otro material. Todo esto depende de la estructura química de la sustancia. Las sustancias no polares o poco polares se disuelven en disolventes no polares o poco polares. En cambio, las sustancias muy polares se disuelven en disolventes muy polares. Los derivados del petróleo son poco polares por ejemplo la gasolina y el icopor. El poliestireno es poco polar y sabemos que la gasolina tampoco lo es por lo tanto al juntarlos el poliestieno se disuelve en la gasolina.
I. Al ejecutar el experimento se puede evidenciar que ambos materiales al entrar en contacto generan una reacción la cual se refleja a través de burbujas.
II.

¿COMO OBTENER HONGOS COMESTIBLES?
PLANTEAMIENTO DEL PROBLEMA:
Las proteínas que contienen los alimentos extraídos de los animales causan algunos daños en el organismo, los cuales se pueden reemplazar por las proteínas vegetales ya que estas son mejores y no causan daño, estas se pueden encontrar en hongos comestibles cultivados en casa.
OBJETIVOS
GENERAL: Mostrar una alternativa a las personas para que cambien el hábito de consumir proteínas animales por las vegetales. Por medio de los hongos GIRGOLA (Orellana)
ESPECÍFICOS:
· Agregar algunos compuestos al sustrato los cuales (hoja de caña seca, pasto seco, aserrín, cal, cúrcuma y salvado de trigo) ayudaran a que el hongo contenga más nutrientes.
· Enseñar a las personas como cultivar hongos comestibles en casa.
· Obtener los nutrientes necesarios para reemplazar las proteínas por medio de la GIRGOLA.
JUSTIFICACIÓN
Hongos comestibles es un proyecto que se creó por desconocimiento ya que no sabíamos nada acerca de esto. Poco a poco se fue investigando y nos pareció muy importante porque nos dimos cuenta que los hongos tenían grandes beneficios que le ayudaran mucho a los seres humanos en su mejoramiento de la digestión y varias cosas que a diario causan daño.
A parte de todo este tipo de alimento tiene la capacidad de suplantar las proteínas, aumentar el nivel de vitamina D, B1, B2, C y niacina. De igual forma ayudar a diferentes sistemas del organismo, viendo que este alimento ha sido destacado por superar la cantidad de proteínas que tiene cualquier otro vegetal también haciendo parte de uno de los aliados excepcionales para mejorar la salud humana y ambiental. (DIETAS.NET.tu portal de salud y bienestar, 2009)
De igual manera los compuestos con los que son fabricados (agua, proteínas, hidratos de carbono y grasas) ayudan a que este tipo de hongo tenga la cantidad suficiente de aminoácidos esenciales que el organismo requiere para funcionar correctamente, no debemos olvidar que los hongos nos aportan minerales como los son: el cobre, el yodo, el magnesio, el zinc, el potasio y otros. Además en el contexto nacional no se tiene en cuenta el consumo de hongos ya que las personas no tienen la información suficiente acerca de cuáles son sus beneficios, la rápida accesibilidad al momento de poder crearlos y remplazarlos por varios alimentos que le hacen daño a la humanidad.